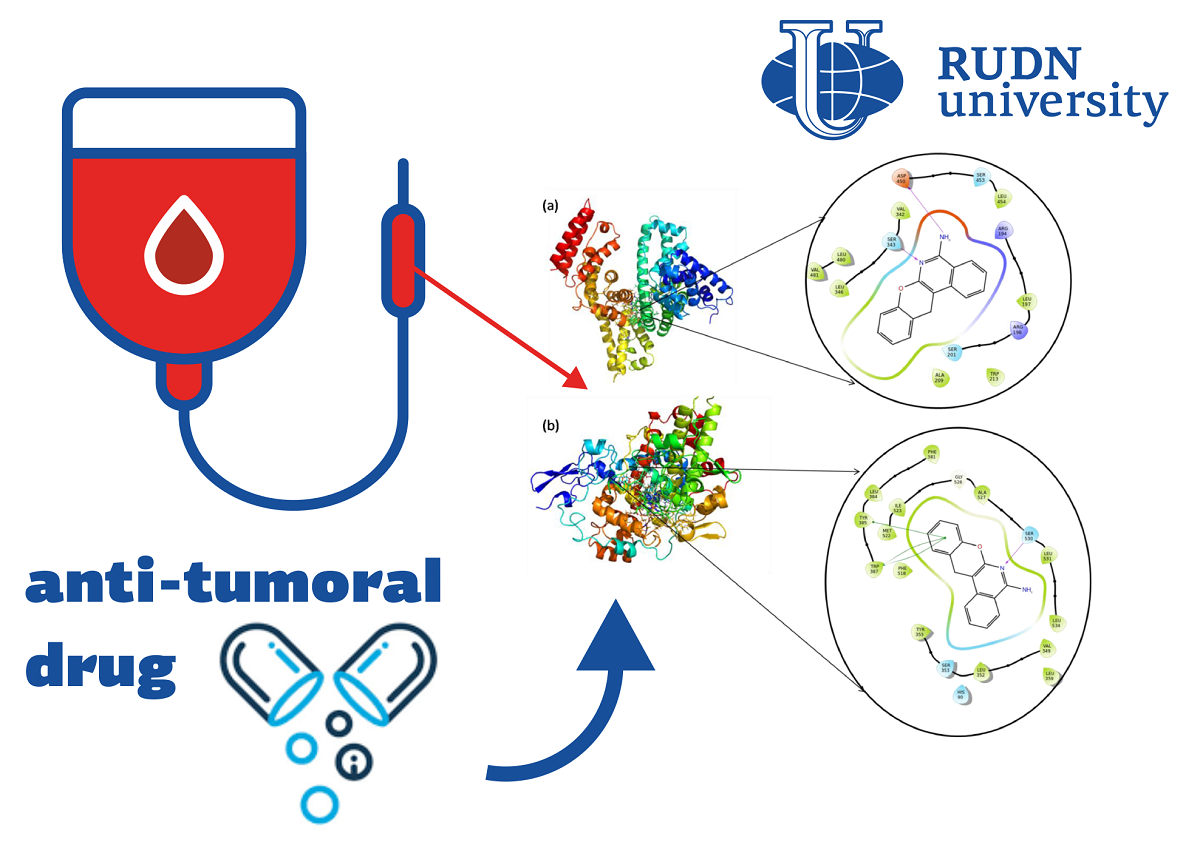
Químicos de RUDN han demostrado cómo un nuevo fármaco antitumoral interactúa con las proteínas de la sangre
Los compuestos heterocíclicos, en los que hay varios «anillos» orgánicos con átomos de otros elementos, son de interés para los químicos y farmacéuticos debido a una amplia gama de actividad biológica. Anteriormente, la Universidad RUDN creó un compuesto heterocíclico con un efecto antitumoral pronunciado. En estructura, se asemeja a los medicamentos aftazol y panoprofeno, que generalmente se utilizan para combatir la inflamación. Al mismo tiempo, el mecanismo de su acción no es completamente conocido por los científicos. Uno de los indicadores de la efectividad del medicamento es su unión a las proteínas de la sangre, por lo que el estudio de este proceso es importante para comprender el trabajo del medicamento. Los químicos de RUDN continuaron estudiando el nuevo medicamento y estudiaron las características de su interacción biofísica con el cuerpo. Para hacer esto, investigaron cómo el medicamento se une a la proteína ciclooxigenasa-1 (PTGS1) y la albúmina sérica bovina (BSA).
«Dado quelas moléculas del compuesto farmacológico creado son similares a los medicamentos comerciales pranoprofenom y aphthazole,es interesante comprender el mecanismo de su interacción de unión con PTGS1 utilizando varios métodos biofísicos. Comprender la interacción con BSA es importante porque es un modelo bien conocido de moléculas de proteínas a, que puede tomar varios medicamentos y transferirlos a un entorno molecular determinado», — Alexey Festa, Candidato de Ciencias Químicas, Profesor Titular en el Departamento de Química Orgánica de la Universidad RUDN.
Los químicos investigaron la interacción del fármaco con BSA y PTGS1 de forma experimental y teórica, utilizando espectroscopia de fluorescencia (fluorimetría),así como modelos moleculares por computadora. La fluorimetría le permite determinar la concentración de una sustancia por la intensidad de la fluorescencia, que ocurre cuando se irradia con una sustancia.
La espectroscopia de fluorescencia mostró que cuando el fármaco interactúa con la albúmina, se produce el efecto del llamado enfriamiento estático. Esto significa que las sustancias se han combinado entre sí, y seobtiene un producto natural sin flúor. Este efecto (junto con los resultados de la simulación teórica posterior) sugiere que el compuesto sigue el principio de interacción hidrofóbica. Determina cómo se verá la estructura del compuesto como resultado. El modelado molecular utilizando el método de acoplamiento molecular mostró que, junto con BSA y PTGS1, el fármaco es estable durante todo el tiempo de simulación.
«Los estudios de acoplamiento molecular muestran que el fármaco tiene una buena capacidad de unión tanto en combinación con BSA como en combinación con PTGS. Al mismo tiempo, la energía teóricamente calculada de la conexión casi coincide con la calculada experimentalmente.El análisis dela dinámica molecularmuestra que el fármaco es estable tanto en el sistema complejo con BSA como en el sistema con PTGS1» — Cubramani Kartikean, postdoc Departamento de Química Orgánica de la Universidad rudn.
Los resultados se publican en el Journal of Molecular Structure.
El primer ganador del Premio Internacional Universidad Rusa de la Amistad de los Pueblos Patrice Lumumba por logros científicos y méritos en el campo de las matemáticas, dotado con 5 millones de rublos, fue el científico de San Petersburgo, Sergei Ivanov.
Los productos derivados de las microalgas constituyen un avance en el campo de la bioeconomía. Las posibilidades de los biorrecursos se debatieron en el seminario internacional de investigación «Fundamentos para una energía verde sostenible»(«Foundations for a Green Sustainable Energy») en el marco del Grupo Temático Internacional «Energía» de la Universidad de Red BRICS. El evento fue organizado por el Instituto de Ecología de la RUDN.
El año 2024, en la RUDN empezó a admitirse las solicitudes de candidatura para el nuevo Premio anual a los logros científicos en el campo de la química. El premio se creó para reconocer las contribuciones a la investigación fundamental y aplicada, así como los méritos en la consecución de los Objetivos de Desarrollo Sostenible de la ONU.